Sul modello della parola Genomica, che si riferisce allo studio dell’intero genoma, lo studio delle proteine è stato denominato “Proteonomica”. Con questa voce si intende lo studio della struttura e delle funzioni delle proteine e di come le proteine si associano, in maniera stabile o solo temporanea, per assolvere le varie funzioni cellulari.
Ma il genoma è piuttosto costante mentre il Proteoma è in continuo cambiamento per via delle interazioni con l’ambiente e con il genoma. In un organismo l’espressione delle proteine è radicalmente differente nelle diverse parti del corpo, nei differenti stadi della sua vita e nelle diverse condizioni ambientali.
Una scoperta dovuta al Progetto Genoma Umano è che il numero dei geni che codificano per una proteina è di circa 22.000, mentre il numero di proteine è di circa 400.000. Il grande aumento del numero delle proteine è dovuto, si pensa, a fattori come lo splicing.
http://it.wikipedia.org/wiki/Proteine
http://it.wikipedia.org/wiki/Splicing
Le proteine quindi non lavorano da sole, ma si associano in grandi complessi multiproteici, alcuni dei quali hanno le caratteristiche di macchine piuttosto complesse che regolano la sintesi e degradazione di altre proteine, l’invio di segnali tra una cellula e l’altra e così via.
La morfologia del complesso proteico è determinata con la cristallografia a raggi X o con la risonanza magnetica o, come descritto nell’articolo, con l’Atomic Force Microscopy (AFM).
http://www.cnrs.fr/cw/en/pres/compress/supercomplexe.htm
La definizione globulare o filamentosa dipende dalla struttura e riflette la forma del complesso. Non è detto che il complesso abbia la stessa struttura delle proteine che la compongono. Ad esempio i microtubuli, che sono filamentosi, sono formati da proteine globulati: la α e β tubulina.
http://it.wikipedia.org/wiki/Microtubuli
Esempi di complessi globulari sono:
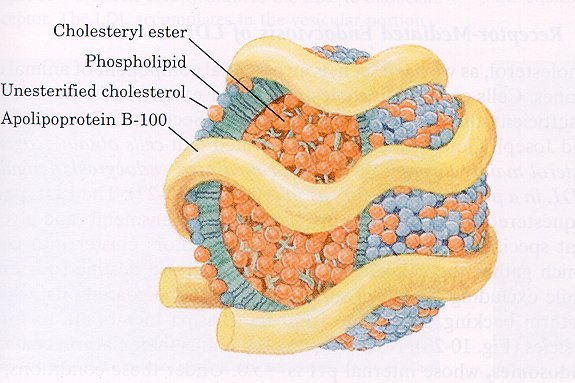
le lipoproteine: l’unione con le proteine ne facilita il trasporto nei liquidi dell’organismo;
da: http://walzemlab.tamu.edu/lipoprotein.html
la famiglia di proteine MCM (Mini-Chromosome Maintenance) nel lievito;
http://www.cnr.it/istituti/ArticoliJCR.html?cds=007&id=30227
http://arjournals.annualreviews.org/doi/full/10.1146/annurev.biochem.68.1.649
la condensina e la coesina
http://www.jcb.org/cgi/content/full/156/3/419
http://www.cellbio.duke.edu/Faculty/Erickson/pdf’s/Anderson%20condensinCohes.pdf
Altri complessi sono:
complesso filamentoso dei GroEL and GroES, facilitano il folding delle proteine;
http://web.unife.it/progetti/biologiamolecolaredellemostasi/chaperoni.html
http://www.bioinformaticscourses.com/ISB/sp2003/1AON/GroELS.ppt
complessi della Polimerasi II per la sintesi del RNA;
http://www.vialattea.net/esperti/php/risposta.php?num=10949
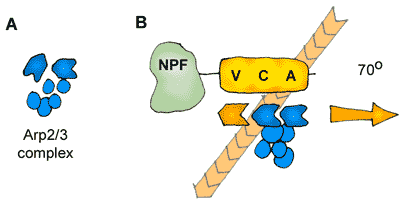
complesso ARP2/3 crescita dei filamenti di actina;
http://en.wikipedia.org/wiki/Arp2/3_complex
complesso mTOR, trasmissione segnali nella via metabolica che regola la massa cellulare;
http://web.wi.mit.edu/sabatini/pub/research_MTORsignal.html
complesso E2F-6 controllo della trascrizione, regolazione del ciclo di divisione cellulare;
http://mcb.asm.org/cgi/content/abstract/12/10/4327
Immagine del complesso Arp2/3 da: http://www.bris.ac.uk/biochemistry/cory/resarp.html
Per approfondire:
http://www.torinoscienza.it/articoli/apri?obj_id=66
http://www.odv.bo.it/2004-1//notiziario-02.pdf
http://www.genomenewsnetwork.org/articles/01_02/Yeast_proteins.shtml
http://bioinformatics.oxfordjournals.org/cgi/content/full/22/7/823